|
Quando tutta l’acqua è stata rimossa quello che resta si può assimilare ad un corpo composto da particelle sottilissime, una sorta di polvere secca tenuta insieme solo da forze superficiali. Al crescere della temperatura, iniziano a svilupparsi legami chimici tra le particelle.
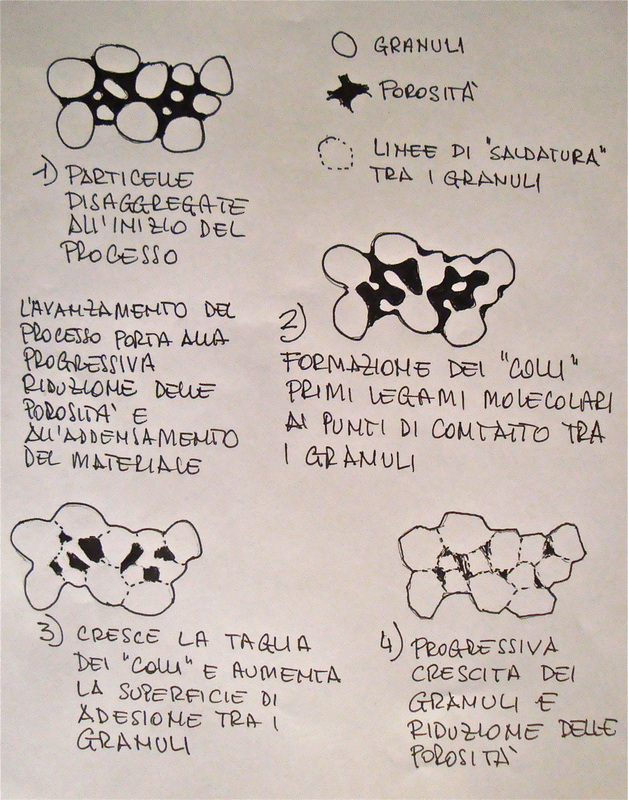
Provando a dirlo in modo estremamente semplificato, avviene un movimento di atomi da un granulo all’altro ed entrando in contatto generano legami tra granulo e granulo. Il materiale non ha ancora raggiunto al temperatura di fusione. Come risultato dell’incremento energetico dovuto all’aumento della temperatura, avviene una riorganizzazione della struttura molecolare. Questo processo si chiama sinterizzazione. In generale la sinterizzazione può avvenire sia per incremento della pressione che della temperatura. La seconda modalità è quella che, normalmente, riguarda la ceramica (processo termico). Sempre in via generale, la sinterizzazione trasforma un materiale polverulento in un corpo coeso e indivisibile e consiste essenzialmente nella rimozione della porosità tra le particelle della polvere di partenza (addensamento), combinata con la formazione di robusti collegamenti (colli) tra di esse col risultato di un complessivo ritiro del volume di partenza e la fusione tra loro dei microgranuli in grani via via più grandi (coalescenza e sviluppo di forti legami tra particelle adiacenti). Dal punto di vista meccanico la chiusura dei pori e la fusione dei microgranuli di partenza hanno come conseguenza l’incremento della resistenza e della tenacità del materiale di partenza. Un esempio classico di sinterizzazione è la pasticca di aspirina. Il trattamento termico avviene ad una temperatura più bassa della temperatura di fusione del materiale trattato (o del punto di fusione del principale componente nel caso di una miscela). Tornando alla ceramica: introducendo dell’argilla in polvere nel forno e cuocendo fino alla temperatura necessaria a trasformare l’ammasso sciolto in una massa coesiva solida – il punto di sinterizzazione generalmente corrisponde al calore rosso – si ottiene un materiale indifferente all’acqua, quindi resistente allo slaking (disaggregazione delle particelle nell’acqua). Se scaldata ulteriormente la ceramica evidenzierà un'ottima resistenza agli shock termici, proprietà che si perderà in egual misura nella fase vetrosa sviluppata alle alte temperature. Nei laboratori di ceramica generalmente non si utilizza la polvere ma un impasto semiliquido (slurry), per la foggiatura a colaggio, oppure una miscela plastica lavorata con le mani o al tornio; è chiaro che è proprio la presenza dell'acqua che rende l'argilla plastica e perciò lavorabile; una volta asciugata fino a durezza osso e quindi essiccata durante le prime fasi di cottura, l'argilla, come detto all'inizio, si può effettivamente considerare un corpo costituito da particelle microscopiche secche (come la polvere). Se si ha a che fare con miscela di materiali diversi, la temperatura di sinterizzazione è talvolta al di sopra del punto di fusione di una delle componenti minori (ma non della componente principale, come già detto) il che comporta una sinterizzazione in fase liquida. Una delle componenti della miscela entra, cioè, in fase liquida e pentera nella porosità interstiziale. Ciò si traduce in tempi più brevi rispetto alla sinterizzazione allo stato solido. In ceramica abbiamo a che fare con questo tipo di sinterizzazione. La maggior parte delle argille commerciali sono, infatti, degli impasti, inoltre, anche le argille naturali, oltre agli alluminosilicati possono contere carbonato di calcio, ferro e altre impurità in percentuali anche importanti; di fatto si comportano come delle miscele. Poi, mano a mano che il processo di fusione prende piede il processo di cottura si evolve in nuove fasi di cui parleremo in seguito. Di seguito un disegno schematico per illustrare cosa avviene all’interno dell’ammasso.
0 Comments
Leave a Reply. |
AutoriVesuvioLab Archivio
Ottobre 2023
Categorie
Tutti
|

 Feed RSS
Feed RSS